Untuk perspektif jangka panjang, inovasi pembuatan vaksin berbasis sel dendritik perlu diberi ruang dan peluang tanpa mengurangi kaidah-kaidah ilmiah yang obyektif.
Dalam beberapa bulan terakhir ini Indonesia mengimpor vaksin untuk Covid-19 dari beberapa negara dalam jumlah yang besar. Vaksin Covid-19 yang telah dan sedang dalam proses evaluasi untuk masuk ke Indonesia adalah Sinovac, AstraZeneca, Moderna, Pfizer, Sinopharm, dan Sputnic V.
Semua vaksin tersebut diimpor dalam bentuk finish product (produk jadi), kecuali sebagian vaksin Sinovac yang bulk-nya diimpor dari China kemudian diproduksi dan dikemas oleh PT (Persero) Bio Farma. Penelitian dan uji klinis semua vaksin tersebut dilakukan di negara pembuatnya.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
Hanya vaksin Sinovac sebagian uji klinis tahap 2 dilakukan di Indonesia. Izin edar vaksin-vaksin ini di Indonesia semua berbasis emergency use authorization (EUA) atau izin penggunaan darurat.
Vaksin Covid-19 yang diimpor sebagian berbasis platform antigen yang dilemahkan/dimatikan. Beberapa vaksin memiliki bahan dasar yang berbeda: Pfizer dan Moderna menggunakan bahan dasar mRNA dan AstraZeneca menggunakan viral vector.
Platform vaksin konvensional Covid-19 memang sangat berbeda dengan platform vaksin Nusantara yang berbasis pada sel dendritik (dendritic cell). Oleh karena itu, regulasi dan standar pembuatan kedua vaksin tersebut dalam implementasinya terdapat beberapa perbedaan.
Apabila tidak memahami keduanya, maka sulit untuk dipertemukan karena berbeda platform ataupun proses teknologinya.
Vaksin konvensional
Prosedur pembuatan vaksin Covid-19 dengan platform virus yang dilemahkan dan mRNA cukup rumit dan memerlukan waktu yang sangat panjang.
Apabila ditempuh prosedur normal, pembuatan vaksin konvensional tersebut, mulai dari penelitian awal sampai dengan uji klinis tahap 3, memerlukan waktu dari sepuluh tahun hingga 15 tahun.
Organisasi Kesehatan Dunia (WHO) dengan alasan darurat pandemi mendorong agar proses evaluasi dan penggunaan vaksin Covid-19 dapat dipercepat melalui skema EUA. Dewasa ini WHO memiliki daftar vaksin Covid-19 sekitar 31 vaksin yang telah dirilis ataupun yang sedang dalam tahap uji klinis.
Sebagai gambaran dapat dicermati bagaimana perusahaan biofarmasi Sinopharm (China) mengembangkan vaksin Covid-19 dari virus tak aktif yang disebut BBIBP-CorV. Para peneliti mempelajari sampel virus SARS-CoV-2 yang berasal dari tiga orang, kemudian memilih satu di antara ketiga sampel untuk bahan dasar vaksin.
Virus tersebut kemudian dikembangkan dalam sel dengan menggunakan bahan kimia yang disebut beta-propiolakton untuk menonaktifkan virus. Bahan ini mengubah materi genetik virus sehingga tidak bisa bereplikasi.
Perusahaan lain yang menggunakan virus inaktif melakukan pendekatan hampir serupa. Para ilmuwan di Sinovac (China) mengembangkan vaksin Covid-19 dari virus yang dinonaktifkan yang disebut CoronaVac. Bharat Biotech dan Dewan Riset Medis India mengembangkan Covaxin.
 Untuk meningkatkan efektivitasnya, vaksin-vaksin ini mengandung aluminium hidroksida, yang berfungsi sebagai adjuvant. Untuk meningkatkan efektivitasnya, vaksin-vaksin tersebut diberi tambahan toll-like reseptor (TLR) 7/8 agonis untuk memicu respons imun menjadi lebih kuat.
Untuk meningkatkan efektivitasnya, vaksin-vaksin ini mengandung aluminium hidroksida, yang berfungsi sebagai adjuvant. Untuk meningkatkan efektivitasnya, vaksin-vaksin tersebut diberi tambahan toll-like reseptor (TLR) 7/8 agonis untuk memicu respons imun menjadi lebih kuat.
Sebelum diproduksi dan dipasarkan, vaksin harus melewati kajian eksplorasi dan serangkai uji klinis yang panjang. Peneliti harus melakukan kajian eksplorasi melalui penelitian di laboratorium untuk mengetahui antigen alami atau sintetik untuk merangsang pembentukan antibodi dalam tubuh.
Setelah itu dilakukan uji praklinis dengan memberikan vaksin kepada hewan percobaan untuk mengetahui efektivitas dan keamanannya serta untuk mengetahui efek samping yang mungkin ditimbulkannya.
Setelah uji praklinis diselesaikan, selanjutnya dilakukan uji klinis tahap 1 sampai tahap 3 yang memerlukan waktu cukup lama dan biaya yang besar. Apabila serangkaian uji klinis tersebut hasilnya positif dan telah mendapat izin edar dari otoritas pemerintah, vaksin baru tersebut boleh diproduksi dan diedarkan untuk digunakan oleh masyarakat luas.
Tidak mustahil, setelah dilakukan uji klinis secara lengkap dan digunakan oleh masyarakat, terjadi kasus yang merugikan kesehatan pasien pada tingkat ringan, sedang, dan serius (kejadian ikutan pasca-imunisasi/KIPI). Vaksin AstraZeneca tercatat telah menimbulkan kasus pembekuan darah di otak terhadap beberapa orang subyek dan menimbulkan kematian di Australia.
Beberapa kasus serius terjadi di Denmark yang menyebabkan pemerintah menghentikan sementara penggunaan vaksin AstraZeneca di negara itu.
Vaksin Nusantara
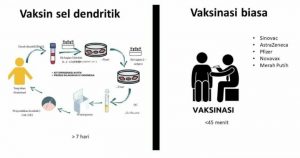
Sangat berbeda dengan pembuatan vaksin konvensional Covid-19, pembuatan vaksin Nusantara tidak memasukkan virus korona nonaktif ke tubuh penerima. Vaksin Nusantara dibuat melalui tahapan yang berbeda dengan vaksin konvensional Covid-19.
Pertama-tama, diambil darah dari tubuh seorang subyek/pasien. Selanjutnya darah tersebut dipisahkan antara sel darah putih dan sel dendritik (bagian dari sel darah putih). Sel dendritik ini akan dipertemukan dengan rekombinan antigen di laboratorium sehingga memiliki kemampuan untuk mengenali virus SARS-CoV-2.
Sel dendritik ini mempunyai memori untuk mengenali dan melawan SARS-CoV-2. Setelah sel berhasil mengenali virus korona, sel dendritik akan kembali diambil untuk disuntikkan ke dalam tubuh pasien yang sama dalam bentuk vaksin. Dengan diberikan vaksin ini, diharapkan pasien memiliki kekebalan atau antibodi dalam melawan Covid-19.
Dari proses pengambilan darah, laboratorium, hingga akhirnya menjadi vaksin yang siap disuntikkan, perlu waktu satu minggu. Dengan pendekatan sel dendritik ini, vaksin tak mengandung virus korona yang sudah dilemahkan, seperti vaksin konvensional Covid-19 lain.
Setelah vaksin diinjeksikan ke tubuh pasien, akan memicu sel-sel imun lain untuk membentuk sistem pertahanan terhadap virus penyebab Covid-19.
Kelebihan vaksin Nusantara: tak ada komponen virus yang turut disuntikkan ke dalam tubuh, sebab proses pengenalan sel dendritik dengan rekombinan antigen virus dilakukan di luar tubuh, yaitu di laboratorium. Selain itu, karena komposisi autolog yang personal, pasien hanya menerima suntikan vaksin yang berasal dari sel darahnya sendiri, bukan orang lain.
Vaksin lain dengan platform dendritik yang sudah dirilis pada 2009 untuk terapi penyakit kanker yang dibuat Debdreon Corp (PROVERENGE) telah disetujui oleh FDA Amerika Serikat. Konsep dan teknologi vaksin dendritik untuk kanker ini serupa dengan vaksin dendritik untuk Covid-19.
Proyek percontohan
Vaksin Nusantara dapat dibuat di laboratorium, rumah sakit, atau klinik dengan peralatan dan kemampuan yang memenuhi standar internasional. Produksi dapat dilakukan secara massal, tetapi tidak dalam suatu fasilitas industri farmasi. Untuk memproduksi dalam skala besar, perlu tenaga yang terlatih serta peralatan dan perlengkapan yang memenuhi standar yang dipersyaratkan.
Standar good laboratory practices (GLP), good clinical practices (GCP), dan good manufacturing practices (GMP) mesti diberlakukan sesuai dengan lingkup teknikal pembuatan vaksin Nusantara. Khusus uji praklinis, jika di luar negeri telah dilakukan dengan hasil yang dapat dipertanggungjawabkan secara ilmiah, maka uji praklinis di Indonesia tak perlu dilakukan.
Laporan uji praklinis itu dapat diserahkan kepada otoritas Pemerintah Indonesia. Dalam pembuatan vaksin Nusantara diberlakukan uji klinis tahap 1 sampai dengan tahap 3 dengan protokol berbasis ilmiah yang dapat dipertanggungjawabkan.
Pada tahap awal diperlukan semacam proyek percontohan untuk kemudian dievaluasi dengan saksama oleh tim ahli yang relevan. Apabila proyek percontohan yang sedang dijalankan RSPAD hasilnya positif untuk melawan Covid-19, dapat direplikasi oleh rumah sakit lain yang memiliki kemampuan dan fasilitas yang dipersyaratkan.
Untuk perspektif jangka panjang, inovasi pembuatan vaksin berbasis sel dendritik perlu diberi ruang dan peluang tanpa mengurangi kaidah-kaidah ilmiah yang obyektif. Selama ini mungkin ada kelemahan dalam pembuatan vaksin dendritik, tetapi ada sisi positif yang dapat dikembangkan untuk kepentingan nasional dan kemanusiaan.
Sampurno Direktur Perum Bio Farma 1994-1996, Dirjen POM 1998-2001, Kepala Badan POM RI 2001-2006
Editor: YOHANES KRISNAWAN
Sumber: Kompas, 19 April 2021