Korosi (perkaratan) terjadi dimana-mana dimuka bumi kita, sedikit sekali bahan yang tak terjamah korosi. Beberapa contoh adalah platina, mas dan gelas. Apakah korosi atau proses perkaratan itu? Salah satu definisi korosi adalah berkurangnya kualitas suatu bahan padat oleh reaksi kimia dengan lingkungannya. Marilah kita membatasi pembahasan kita pada korosi logam saja.
Besi berasal dari karat
Kebanyakan logam berasal dari bijih yang terdiri dari oksida logam atau garam logam. Bijih besi amat mirip dengan karat besi! Ini tak mengherankan sebab kebanyakan bijih besi adalah oksida besi yang susunan kimianya seperti karat besi, yaitu Fe2O3. Jadi besi berasal dari karat yang diolah dengan menambahkan energi. Jumlah energi yang sama akan diperlukan untuk mengubah besi kembali menjadi karat. Tiap logam memerlukan energi berbeda untuk memurnikannya. Makin banyak energi yang diperlukan, makin cenderung ia berkarat. Urutan mudahnya berkarat berbagai logarn di air adalah sebagai berikut: magnisium mudah karat, aluminium (murni), zinc (n), besi, timah putih, dan timbal (sulit berkarat).
 Pemurnian suatu logam adalah bagaikan mendorong bola pada tanjak-an. Bila bola dilepaskan maka energi yang terkandungnya akan menyebabkan bola menggelinding turun, menggunakan energi simpannya. Upaya pengendalian korosi dapat dibayangkan sebagai usaha untuk mencegah agar bola tidak turun lagi. Untuk ini diperlukan energi, yang juga berarti biaya.
Pemurnian suatu logam adalah bagaikan mendorong bola pada tanjak-an. Bila bola dilepaskan maka energi yang terkandungnya akan menyebabkan bola menggelinding turun, menggunakan energi simpannya. Upaya pengendalian korosi dapat dibayangkan sebagai usaha untuk mencegah agar bola tidak turun lagi. Untuk ini diperlukan energi, yang juga berarti biaya.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
Sebetulnya peristiwa ini adalah salah satu penjelmaan prinsip dasar alam kita, yaitu bahwa bila alam dibiarkan sendiri akan cenderung ke-pada keadaan yang paling berantakan. Prinsip ini sering dikenal sebagai hukum termodinamika ketiga.
Sel Korosi
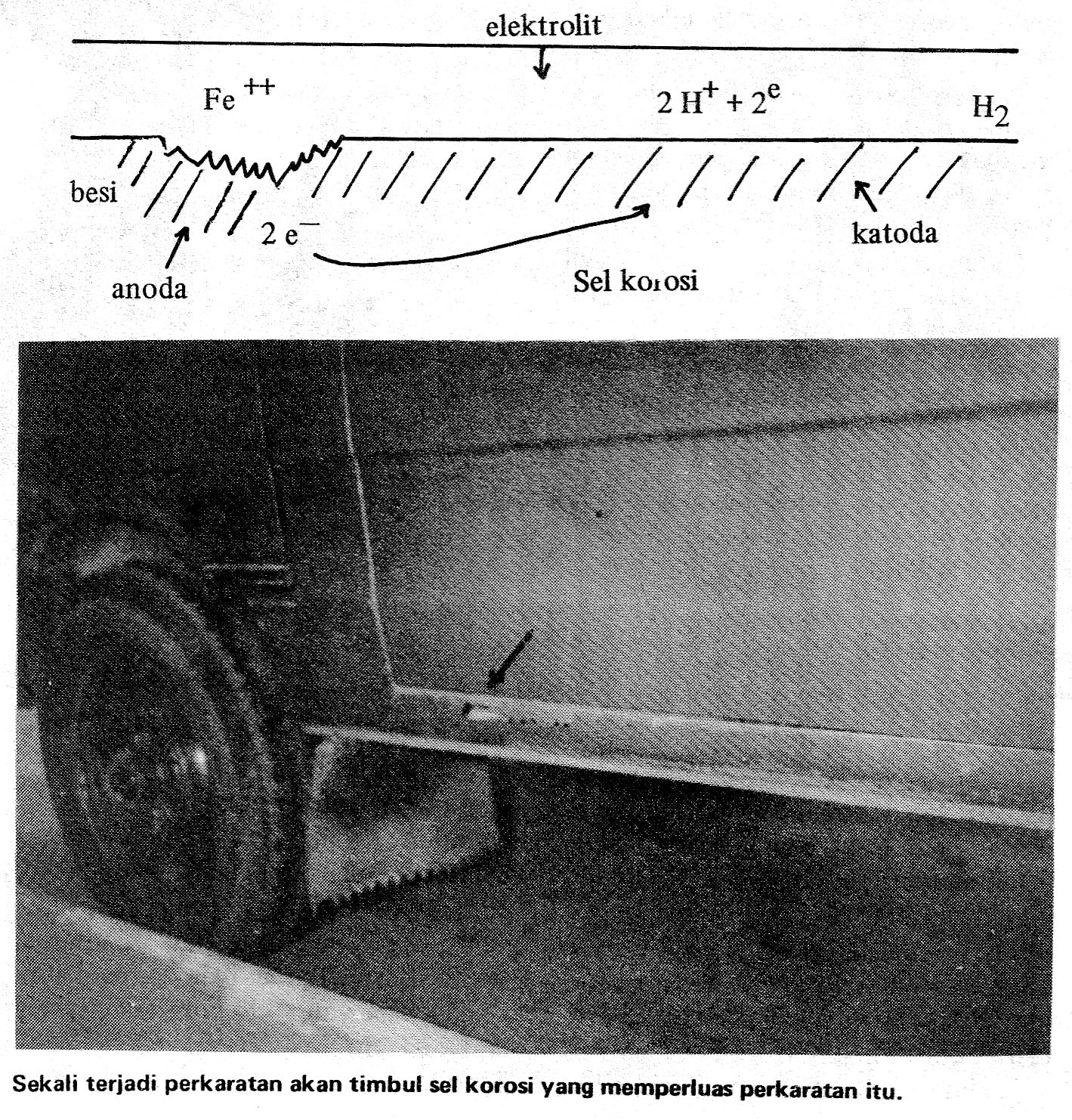
Kita dapat memahami peristiwa korosi dengan gambaran berikut. Bila permukaan logam terlapisi zat cair yang dapat menghantar listrik disebut elektrolit, misalnya air garam, maka atom pada bagian permukaan logam dapat melarut sebagai ion, meninggalkan elektron. Pada bagian ini dikatakan terjadi oksida. Bagian ini akan membentuk anoda (kutub positif dari suatu sel listrik, seperti pada baterei. Bagian lain dari logam akan berlaku sebagai katoda (kutub negatif) yang menarik elektron yang dihasilkan anoda. Dikatakan elektron akan diambil oleh ion positif yang ada didalam elektrolit. Peristiwa ini ditunjukkan pada gambar dibawah. Anoda, elektrolit, dan katoda dikatakan membentuk sel korosi. Tanpa adanya elektrolit proses korosi tak terjadi oleh sebab rangkaian listrik menjadi terputus. Sifat-sifat fisik elektrolit seperti daya hantar listrik, suhu, macam dan jumlah gas terlarut sangat berpengaruh terhadap kecepat-an korosi.
Di fihak lain sifat fisik bahan yang terkorosi, seperti keserbasamaan struk-tur dalam bahan, adanya bahan lain, dan potensialnya terhadap elektrolit akan berpengaruh besar pda kecenderungan dan kecepatan korosi.
Berbagai Peristiwa Korosi
Gambaran di atas memudahkan kita untuk berfikir tentang berbagai peris- tiwa korosi. Dari segi elektrolit daya hantar listrik dan macam serta jumlah gas terlarut amat berperan. Korosi pada baja di pantai adalah 400 hingga 500 kali lebih besar dari pada di padang pasir. Bangunan baja pada jarak 20 m dari tepi pantai berkarat 12 kali lebih cepat dari untuk jarak 200 m. Biang keladinya adalah natrium khlorida alias garam dapur yang terbawa penguapan air laut. Udara kawasan industri lebih korosif dari pada udara daerah luar kota oleh adanya oksida belerang dari pembakaran bahan bakar. Diantara berbagai gas terlarut oksigen adalah yang paling ganas. Oksigen sendiri dapat mengoksidasi ion besi. Dan sekali terjadi karat, proses korosi makin lancar.
Sejumlah kecil tembaga (kira-kira perpuluhan prosen) menambah daya tahan baja terhadap korosi udara oleh karena terbentuk lapisan tipis oksida pelindung yang tak mudah lepas. Sejumlah kecil nikel dan khrom memberikan perlindungan yang sama. Ba-han yang boleh dikatakan sempurna stainless steel atau baja tanpa karat adalah baja yang dibubuhi tak kurang dari 12% khrom (Cr), yang akan membentuk lapisan oksida khrom amat tipis dan menempel amat kuat pada baja sehingga baja tak mudah terkena korosi. Bila lapisan ini luka maka bagian itu dapat terserang korosi. Daya tahannya terhadap korosi adalah stainless steel. Mutu baja, yaitu kebersamaan bagian mikro di dalamnya sangat berpengaruh terhadap korosi. Sambungan oleh las, misalnya, akan menyebabkan terjadinya elektroda korosi yang memperhebat korosi.
Korosi terlindung banyak menyebabkan kerusakan. Peristiwa ini terjadi pada tempat dimana terjadi pengembunan atau pengumpulan air yang tak mudah “kering. Suatu contoh adalah korosi pada bagian dalam pintu mobil. Contoh lain adalah pengembunan di dalam tangki bensin yang tak penuh sehingga air terkumpul pada dasar tangki. Contoh lain lagi adalah terkumpulnya air di bawah cat yang tak menempel bagus pada badan mobil, yang tampak sebagai tonjolan lunak (seperti gelembung) pada cat mobil. Gas yang timbul pada reaksi kimia ini dapat memperluas bagian cat yang lepas sehingga korosi akan melebar. Untuk korosi udara banyak digunakan lapisan pelindung untuk pencegahannya. Prinsip kerjanya adalah melapisi permukaan logam dengan bahan organik yang bersifat isolator, dan melekat kuat pada logam. Dengan lapisan yang tebal dan tak pernah kering oleh karena penguapan kecil, maka rangkaian listrik sel korosi terhambat arusnya.
Dengan demikian korosi pada bagian ini terhambat. Inilah yang banyak dilakukan oleh perusahaan-perusahaan perlindungan terhadap korosi pada mobil.
Perlindungan terhadap korosi juga merupakan masalah besar pada instalasi minyak pipa-pipa logam di bawah tanah, dan kilang-kilang pada industri kimia. Di sini digunakan berbagai cara listrik seperti perlindungan katodik dan anodik. Di Indonesia masalah korosi ini merupakan tugas Lembaga Mineralogi Nasional LIPI yang ada di Bandung.
Sumber: Majalah AKU TAHU/Maret 1983.