Tabel Mendeleyev kini menjadi keharusan dalam ilmu kimia.
Termasuk unsur buatan, kita mengenal seratus lebih unsur kimia. Semua unsur itu dapat diletakkan dalam satu tabel, dikenal sebagai tabel periodik. Disusun dalam urutan massa atom yang menanjak, secara periodik, tabel ini menunjukkan sifat unsur yang bersamaan. Kalau urutan unsur itu disusun mendatar, maka sifat yang bersamaan itu terkelompok dalam lajur yang sama. Tabel periodik ini mengenal delapan lajur, dari lajur I sampai lajur VIII.
 Penyusunan tabel periodik unsur kimia dilakukan da-lam abad yang lampau. Pada saat itu, beberapa ilmiawan melihat adanya perbedaan dan kesamaan di antara sifat unsur kimia yang telah mereka kenal. Berdasarkan sifat unsur itu, mereka mencoba untuk menyusunnya ke dalam suatu tabel. Dan bersama itu, lahirlah beberapa macam tabel, yang mencoba untuk mengungkapkan susunan unsur berdasarkan sifat mereka.
Penyusunan tabel periodik unsur kimia dilakukan da-lam abad yang lampau. Pada saat itu, beberapa ilmiawan melihat adanya perbedaan dan kesamaan di antara sifat unsur kimia yang telah mereka kenal. Berdasarkan sifat unsur itu, mereka mencoba untuk menyusunnya ke dalam suatu tabel. Dan bersama itu, lahirlah beberapa macam tabel, yang mencoba untuk mengungkapkan susunan unsur berdasarkan sifat mereka.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
Dari sejumlah tabel yang ada, yang paling terkenal dan kemudian diakui secara umum, adalah tabel dari Mendeleyev Diumumkan pada tahun 1869, tabel Mandeleyev ini sampai berani meramal sifat dari beberapa unsur yang, pada saat itu, belum dikenal oleh para ilmiawan. Bahkan, tabel ini, juga berani mengoreksi kekeliruan pada data sifat unsur yang telah diukur oleh para ilmiawan zaman itu.
Bermacam Unsur
Para seniman pertukangan zaman kuno telah mengenal sejumlah unsur. Mereka mengenal emas, perak, tem-baga, besi, air raksa, timbal, timah, belerang, dan arang. Emas dan perak, sering diperlakukan sebagai logam ber-harga, dan digunakan sebagai mata uang. Tembaga dan besi, digunakan sebagai bahan pembuat alat, termasuk alat perang. Sedangkan air raksa, banyak diutak-utik untuk pembuatan obat.
Kemudian, para alkemi (ahli kimia zaman dahulu), menambah jumlah itu dengan beberapa unsur lagi. Pada zaman ketika Columbus berlayar ke benua Amerika, Basil Valentin menemukan unsur antimoni atau stibium. Pada tahun 1530, Georgius Agricola menemukan unsur bismuth. Peristiwa ini ditulis dalam bukunya yang berjudul De Re Metallica.
Dalam deretan ini, kita temukan juga Philippus Aurelius Theophratus Bombast von Hohenheim. Dikenal dengan nama panggilan Paracelsus, von Hohenheim memberikan uraian yang cukup terperinci tentang unsur seng. Demikian pula, Brandt menjelaskan sifat unsur fosfor, arsen, dan kobalt. Dan pada tahun 1735, Don Antonio de Ulloa, menemukan unsur platina.
Pada abad 19, sejumlah unsur pun ditemukan lagi oleh para ilmiawan. Mereka menemukan nikel, hidrogen, oksigen, klor, mangan, tungsten(wolfram), krom, molibdenum, titan, tellurium, zirkonium, uranium, dan beimacam-macam lagi. Dengan alat dan cara yang mereka kenal, pada waktu itu, sifat unsur ini mereka catat dan umumkan.
Menjelang tahun 1869, telah dikenal 63 macam unsur. Jurnal kimia mencatat sifat dari 63 unsur ini. Ada sifat unsur yang tercatat dengan lengkap dan jelas, namun ada juga yang belum jelas. Sifat itu, ternyata, bermacam ragam, bergantung kepada sifat apa dari unsur itu yang kita lihat.
Massa atom unsur itu berbeda-beda, beranjak dari 1 sampai 238. Fasanya juga berbeda. Pada keadaan biasa, ada yang berbentuk gas, ada yang berbentuk cairan , dan ada pula yang berbentuk padat. Dari kekerasannya, ada logam yang sangat keras , namun ada juga logam yang lunak. Ada yang berat, dan ada pula yang ringan. Warnanya tak kalah bermacam ragam. Ada yang merah, ada yang kuning, ada yang kelabu, serta ada yang putih.
Jika unsur itu digosok, ada yang berkilauan, dan ada pula yang tetap buram. Ada yang mudah berkarat, tetapi ada pula yang sukar dicemar. Dan jika unsur padat dipanasi, tidak semunya mencair dulu, baru kemudian menguap. Tapi, ada yang langsung saja menguap. Titik didih serta titik uapnya pun berbeda-beda.
Sifat kimia mereka, ternyata, beraneka ragam. Ada yang bersenyawa dengan hanya satu atom oksigen, ada yang dengan dua, ada yang dengan tiga, dan bahkan, ada yang sekaligus dengan empat atom oksigen. Secara kimiawi, ada yang sangat aktif, tetapi ada juga yang sangat tidak aktif.
Dengan dikenalnya 63 unsur kimia, para ilmiawan melihat adanya 63 kesamaan dan perbedaan sifat, yang mungkin saja memiliki aturan tertentu. Aturan inilah yang mereka cari, sehingga sifat unsur itu tidak lagi tampak seolah-olah kacau balau atau acak saja. Usaha ini, ternyata, tidak mudah. Makin banyak sifat unsur yang diperhatikan di dalam aturan, makin sulit pula mereka menemukan aturan itu.
Hukum Oktaf
Pada tahun 1852, Edward Frankland, seorang ahli persenyawaan organometalik, menyusun teori valensi di dalam ilmu kimia. Teori ini mengemukakan, bahwa setiap jenis atom, mempunyai kemampuan tertentu untuk bersenyawa dengan atom lain. Valensi atom merupakan salah satu sifat unsur yang dapat digunakan untuk menentukan aturan di antara unsur itu unsur-unsur itu.
 Satu dasawarsa kemudian, beberapa ilmiawan lainnya menggunakan teori valensi ini, bersama-sama dengan sifat unsur lainnya, untuk menyusun tabel unsur. Mereka menyusunnya secara tersendiri, satu dan lainnya, tanpa saling mengetahui. Ternyata, susunan mereka memiliki banyak persamaan. Dasar susunan mereka berkisar pada massa atom dan valensinya.
Satu dasawarsa kemudian, beberapa ilmiawan lainnya menggunakan teori valensi ini, bersama-sama dengan sifat unsur lainnya, untuk menyusun tabel unsur. Mereka menyusunnya secara tersendiri, satu dan lainnya, tanpa saling mengetahui. Ternyata, susunan mereka memiliki banyak persamaan. Dasar susunan mereka berkisar pada massa atom dan valensinya.
Pada tahun 1862, seorang ahli geologi yang mempelajari kimia, Alexandre-Emile Beguyer de Chancourtois, mencoba untuk menyusun unsur berdasarkan urutan massa atomnya. Susunan itu dilukiskannya pada permukaan suatu silinder. Pada susunan ini, ia menemukan, bahwa unsur yang memiliki sifat bersamaan, terletak pada garis tegak yang sama.
Hal ini ditulisnya dalam suatu makalah. Susunan in! dinamakannya sebagai heliks tellurik. Sayang, tulisannya itu penuh dengan istilah geologi, sehingga sukar dipahami para ahli kimia. Lagi pula, karena merasa sukar untuk mencetak gambar silinder demikian di atas kertas, penerbit jurnal menghilangkan gambar itu dari tulisan tersebut. Tanpa gambar ini, uraian tentang heliks tellurik itu, tidak lagi tampak jelas.
Makalah ini tidak mendapat perhatian. Dan bersama itu, salah satu susunan unsur yang bersifat periodik, hilang dari ingatan para ilmiawan. Barulah kemudian, jauh setelah tabel periodik Mendeleyev terkenal ke mana-mana, jurnal yang sama menerbitkan gambar silinder heliks tellurik itu.
Tanpa mengetahui karya Beguyer de Chancourtois, pada tahun 1864, John Alexander Reina Newlands menyusun taber unsur berdasarkan urutan massa atomnya. Di hadapan “English Chemical Society” (Masyarakat Ahli Kimia Inggris), di Burlington House, Newlands mengemukakan bahwa, secara berulang, setiap tujuh unsur dapat disusun berurutan. Unsur pada urutan yang sama, kata Newlands, memiliki sifat yang sama pula.
Newlands menyamakan susunan ini dengan susunan kunci piano, yang kembali lagi ke suara sama setelah satu oktaf. Berpegang teguh pada aturan ini, tabel Newlands menunjukkan hukum oktaf di dalam susunan unsur. Kata Newlands, “Anggota dari unsur kelompok yang sama, satu terhadap lainnya, memiliki hubungan yang sama seperti ujung-ujung dari satu atau lebih oktaf di dalam musik.”
Para ahli kimia di London menertawakan hukum oktaf Newlands. Bahkan, secara bergurau, Profesor Foster mengatakan mengapa Newlands tidak menyusunnya saja berdasarkan abjad awal nama unsur itu. Tidak berhasil meyakinkan para ilmiawan, Newlands pun tidak berhasil memuat makalahnya ke dalam jumal. Editor jurnal menolak untuk memuatnya. Dan hukum oktaf lenyap dari perhatian. Baru kemudian, jauh setelah tabel Mendeleyev diterima para ilmiawan, pada tahun 1877, Newlands dianugerahi medali Davy oleh Royal Society.
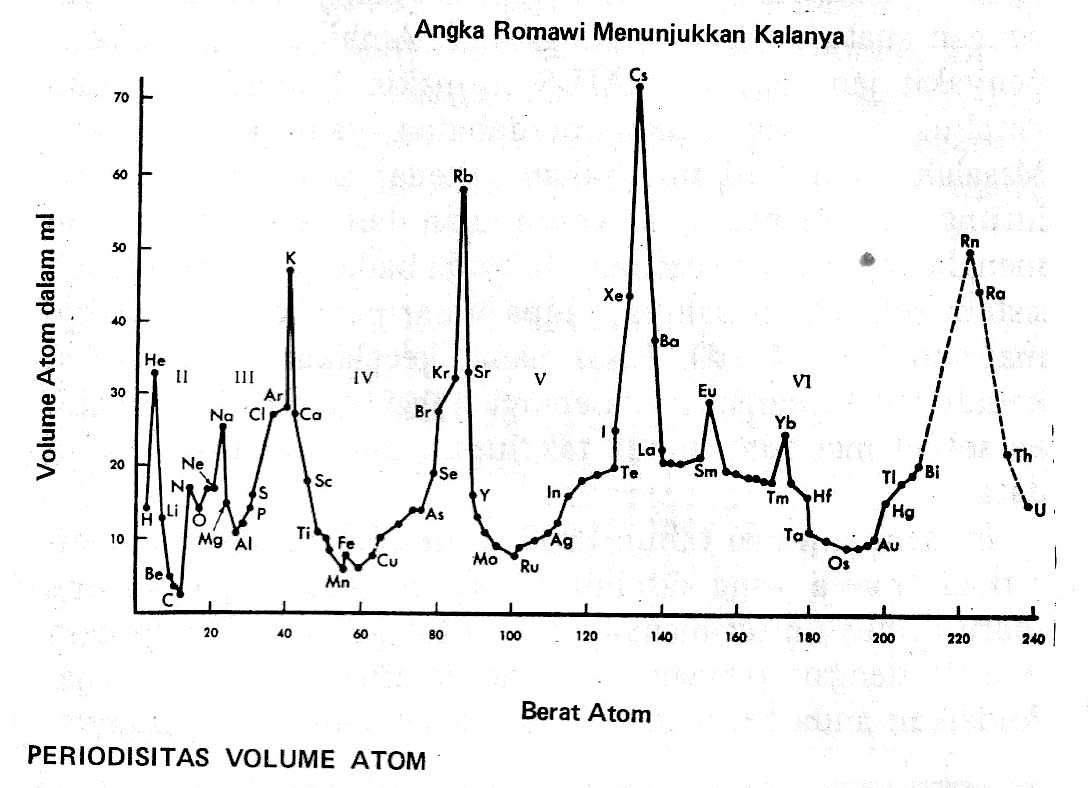
Bersamaan waktu dengan penemuan Mendeleyev, Julius Lothar Meyer juga menyusun tabel unsur. Meyer mencurahkan perhatiannya kepada volume atomik, yakni ruang yang ditempati oleh atom darl unsur bersangkutan. Ia menemukan, bahwa jika volume atomik ini dilukis terhadap massa atom, maka garis yang menghubungkan titik itu akan naik dan turun secara periodik: dua perioda pendek disusul dua perioda panjang.
Asas tabel ini, sama dengan asas valensi yang digunakan Mendeleyev dalam menyusun tabel periodiknya. Namun, Meyer tidak memiliki keberanian untuk mengumumkan penemuannya itu. Lagi pula, berbeda dengan Mendeleyev, ia tidak memiliki keberanian untuk meramal sifat unsur yang belum ditemukan. Penemuan Meyer baru dipublikasikan pada tahun 1870. Dan pada tahun 1882, bersama Mendeleyev,ia juga menerima medali Davy dari Royal Society.
Mendeleyev & Ramalannya
Anak seorang direktur sekolah menengah, Dmitri Ivanovich Mendeleyev dilahirkan di Tobolsk, Siberia, pada tanggal 7 Februari 1834. Ia merupakan anak bungsu dari suatu keluarga besar. Jumlah keluarga itu tidak diketahui dengan jelas, namun diduga terdiri atas 14 sampai 17 anak. Ayahnya meninggal ketika Dmitri masih kecil, sehingga ibunya, Maria Komiloff, yang berdarah Mongol itu, membuka lagi pabrik gelas keluarga guna menghidupi keluarga besar itu. Dari iparnya, politikus yang dibuang ke Siberia, Dmitri memperoleh pelajaran pertama di bidang ilmu alam.
Ketika kebakaran memusnahkan pabrik gelas mereka, ibunya membawa Dmitri ke Moskwa, untuk melanjutkan sekolah ke universitas. Namun, prosedur yang berliku-liku membuat usahanya itu gagal. Kemudian, ibunya membawanya ke St. Petersburg (kini Leningrad), dan memasukkannya ke bagian ilmu alam pada institut pendidikan —institut yang mendidik guru sekolah menengah (semacam IKIP di sini). Di sana, Dmitri mempelajari matematika, fisika, dan kimia.
Mendeleyev lulus sebagai juara kelas. Namun, malang juga menimpa dirinya. Ibunya meninggal tak lama setelah itu. Kesehatan Mendeleyev juga sangat buruk. Dokternya mengatakan, bahwa umur Mendeleyev tinggal enam bulan lagi. Sekalipun demikian, pesan terakhir ibunya menambah semangat hidupnya. “Jangan berilusi,” kata pesan ibunya itu, “terus bekerja, bukan terus berbicara. Dengan sabar, carilah…kebenaran ilmiah.”
Mendeleyev mencari udara yang lebih hangat di selatan. Ia menjadi guru ilmu alam di Simferopol. Kemudian, ia balik ke St. Petersburg, dan bekerja sebagai dosen. Namun, demi kemajuan, ia kemudian mengembara lagi ke Prancis dan Jerman. Di sana, ia bertemu dengan Bunsen dan Kirchhof, serta menghadiri Konggres Kimia Pertama di Karlsruhe. Setelah lulus Doktor, ia kembali ke St. Petersburg, dan menjadi guru besar pada umur 32 tahun.
Setelah banyak membaca tentang kimia, Mendeleyev tertarik kepada sifat-sifat unsur kimia. Ia mencari semua catatan tentang semua sifat dari ke 63 unsur yang dikenal pada waktu itu. Dan Mendeleyev pun mencoba untuk menyusun unsur itu dalam satu urutan tertentu. Pada tahun 1869, di hadapan Himpunan Kimia Rusia, Mendeleyev mengumumkan hasil karyanya. Namun, yang paling mengesankan, adalah ramalannyaitu.
Mendeleyev meramalkan adanya unsur-unsur baru , serta menamakannya sebagai eka-aluminium, eka-boron, dan eka-silikon. Berbagai sifat dan ciri dari unsur itu, juga dikemukakan oleh Mendeleyev, secara terperinci. Para ilmiawan meragukan ramalan Mendeleyev itu.Namun, ada juga ilmiawan yang percaya dan memburunya. Ramalan itu ternyata benar. Pada tahun 1875, Lecoq de Boisbaudran, menemukan eka-aluminium dan menamakannya gallium. Pada tahun 1879, Lars Fredrik Nilson, menemukan eka-boron dan menamakannya skandium. Dan pada tahun 1886, Clemens Alexander Winkler, menemukan eka-silikon serta menamakannya germanium.
Mendeleyev tak hanya bertindak sampai di situ. Secara teoritis, ia mengumumkan, bahwa ada ciri unsur yang diukur secara keliru. Mendeleyev mengatakan, bahwa massa atom tellurium yang tercatat sebagai 128 itu, adalah keliru. Kata Mendeleyev, massa itu harus terletak di antara 123 dan 126, bukan 128. Demikian pula dengan massa atom emas dan platina. Menurut Mendeleyev, letaknya tertukar. Dan, ternyata, Mendeleyev benar.
Tabel Periodik Mendeleyev
Mendeleyev membuat 63 kartu. Di dalam setiap kartu itu, dituliskannya nama dan ciri unsur. Kartu itu dipasangnya di tembok laboratorium, berdasarkan urutan tertentu. Jika urutan itu tidak berkenan di hatinya, letaknya diubah. Awalnya, Mendeleyev menjajarkan kartu berdasarkan massa atom yang menanjak. Namun, pada saat unsur berikut mempunyai beberapa ciri serupa dengan unsur yang ada, kartu itu diletakkan di bawah kartu yang ada. Muncullah tabel periodik di tembok laboratorium, tersusun berdasarkan periodisasi massa.
Tabel pertama ini menunjukkan tujuh lajur. Ditemukan, bahwa semua unsur pada lajur I, bersenyawa dengan oksigen dua terhadap satu. Pada lajur II, satu terhadap satu, pada lajur III, dua terhadap tiga. Dan demikian seterusnya. Dengan demikian, urusan persenyawaan dengan oksigen tertampung pada tabel ini. Mendeleyev tentu gembira, namun ia juga merasa ragu. Sifat lain dari unsur itu pun diteliti lagi. Dan bersama itu, muncul beberapa persoalan.
Persoalan pertama adalah letak tellurium dan iodium . Secara berani, ia menukar letak keduanya, sambil meragu-jan massa atom yang terdapat dalam bacaan yang ada. Kemudian muncul letak emas dan platina. Sekali lagi, Mendeleyev menukar letak keduanya. Dalam tabel ini, Mendeleyev melihat adanya letak kosong. Pada lajur III, di antara kalsium dan titanium, terdapat letak kosong di bawah boron. Pikir Mendeleyev, di situ pasti ada unsur yang merniliki sifat menyerupai boron. Hal serupa juga ditemukan di ba-wah aluminium dan silikon. Dari sinilah muncul ramalan eka-aluminium, eka-boron, dan eka-silikon itu.
Tabel Mendeleyev terdiri atas 7 lajur atau kelompok. Dua puluh lima tahun kemudian, para ilmiawan menemukan lagi satu lajur, yakni lajur VIII yang dinamakan kelompok O. Kelompok ini terdiri atas gas mulia, helium, neon, argon,krypton, xenon, dan radon.
Hidup Mendeleyev memiliki sisi lainnya. Ia bukan hanya ilmiawan, melainkan juga mencampuri politik dengan segala akibatnya. Beberapa kali, secara halus, ia disingkirkan oleh pejabat pemerintah ke tempat-tempat yang jauh. Pemah ia disingkirkan ke Amerika Serikat dengan dalih penelitian ilmiah. Ia juga disingkirkan ke Baku dengan dalih penelitian minyak. Dan bermacam-macam lagi. Ketika memotret gerhana matahari, ia mengendarai balon. Bagi petani Rusia, yang belum pernah mendengar tabel periodik, Mendeleyev lebih dikenal sebagai orang yang “terbang dalam gelembung dan menembusi langit.”
Pada tahun 1906, Mendeleyev nyaris memperoleh Hadiah Nobel. Beda satu suara, ia kalah terhadap Ferdinand Frederic Henri Moissan. Namun, pada tahun 1955, sebagai suatu kehormatan, unsur buatan dengan nomor 101 diberi nama mendelevium.
Oleh Dali S. Naga
Sumber: Majalah AKU TAHU/ Maret 1986