Badan POM mengimbau agar para peneliti vaksin nusantara kembali melakukan uji pre-klinik sebelum uji klinik dijalankan. Data interim dinilai belum memadai untuk dilakukan penelitian uji klinik fase kedua.
Data interim atau data sementara yang diserahkan oleh peneliti dari vaksin Nusantara belum memadai untuk menjadi dasar dilakukan uji klinik fase kedua. Badan Pengawas Obat dan Makanan pun mengimbau agar para peneliti kembali melakukan uji pre-klinik sebelum uji klinik dijalankan.
Kepala Badan Pengawas Obat dan Makanan (Badan POM) Penny K Lukito mengatakan, data interim pada uji klinik fase pertama dari vaksin Nusantara belum cukup untuk menjadi landasan pengembangan vaksin tersebut dilanjutkan ke uji klinik fase kedua. Hal ini karena hasil pengujian belum memadai, antara lain terkait dengan keamanan vaksin, kemampuan vaksin dalam membentuk antibodi, serta pembuktian mutu produk vaksin.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
Ia pun mengatakan, jika penelitian masih dilanjutkan, itu tidak dikoordinasikan dengan Badan POM. “Sudah pasti (kelanjutan pengembangan vaksin Nusantara dengan pemilihan subjek uji klinis fase kedua) tidak (dikoordinasikan dengan Badan POM),” katanya saat dihubungi di Jakarta, Kamis (14/4/2021).
Vaksin Nusantara dikembangkan oleh tim peneliti dari Badan Penelitian dan Pengembangan Kesehatan (Balitbangkes) Kementerian Kesehatan, Rumah Sakit Pusat Angkatan Darat (RSPAD) Gatot Subroto, Rumah Sakit Umum Pusat (RSUP) Dr Kariadi Semarang, dan Universitas Diponegoro. Penelitian ini disponsori oleh PT Rama Emerald atau PT Aivita Indonesia yang bekerja sama dengan Balitbangkes.
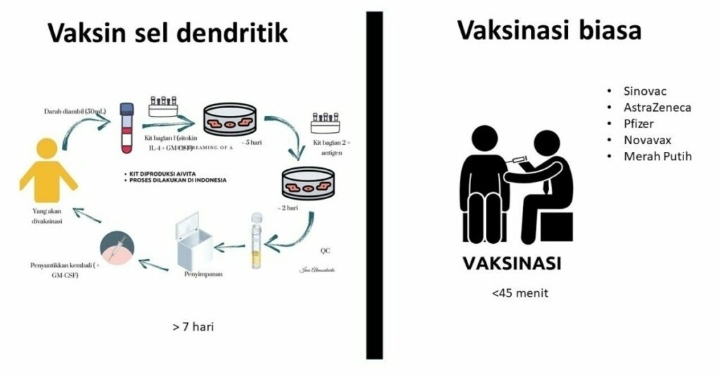
Vaksin tersebut merupakan vaksin yang menggunakan campuran dari sel dendritik yang berasal dari masing-masing orang yang menjadi sasaran vaksinasi, antigen SARS-CoV-2 spike protein (protein paku), dan GMCSF (sarmogastrim) yang menjadi faktor pertumbuhan. Antigen dan GMCSF saat ini belum diproduksi di Indonesia sehingga masih perlu diimpor dari AS.
Penny menuturkan, data pengukuran antibodi IgG (immunoglobulin G) pada studi pre-klinik yang dihasilkan dari pemberian vaksin dendritik tersebut menunjukkan respons antibodi yang tidak konsisten. Respons hanya meningkat pada kelompok hewan yang diberikan kombinasi vaksin denditrik dengan GMCSF. Sementara, tidak ada pengujian pre-klinik yang hanya menggunakan GMCSF saja. Hal ini menimbulkan asumsi, peningkatan antibodi hanya karena pemberian GMCSF bukan karena vaksin dendritik.
Karena itu, ia mengatakan, penelitian vaksin tersebut sebaiknya dikembangkan kembali dengan melakukan uji pre-klinik di Indonesia sebelum masuk ke uji klinik. Ini diperlukan untuk mendapatkan konsep dasar yang jelas dari vaksin sehingga uji klinik di manusia tidak dilakukan tanpa kepastian. Adapun data uji pre-klinik yang dilaporkan ke Badan POM merupakan pengujian yang dilakukan di AS.
“Kegiatan penelitian pre-klinik sebaiknya dilakukan dengan pendampingan dari Kemenristek/BRIN (Kementerian Riset dan Teknologi/Badan Riset dan Inovasi Nasional). Ini sesuai dengan hasil kesepakatan pada RDP (Rapat Dengar Pendapat) DPR RI pada 10 Maret 2021”, tutur Penny.
Berdasarkan hasil inspeksi yang dilakukan oleh Badan POM, sejumlah aspek pada pengembangan vaksin Nusantara juga belum sesuai. Itu antara lain, tidak memenuhi aspek pemenuhan Cara Produksi yang Baik (Good Manufacturing Practices/GMP), aspek Cara Berlabolatorium yang Baik (Good Laboratory Practice/GLP), dan aspek pemenuhan Cara Uji Klinik yang Baik (Good Clinical Practice/GCP).
Dari kedua aspek tersebut setidaknya ditemukan, produk vaksin tidak dibuat dalam kondisi streril, produk akhir vaksin tidak dilakukan pengujian kualitas sel dendritik, serta metode pengujian tidak dilakukan validasi dan standardisasi sebelum penelitian. Ditemukan pula inkonsistensi pencatatan data, serta adanya subjek yang seharusnya tidak masuk dalam kriteria inklusi karena sudah memiliki antibodi tetap tetap diikutkan dalam penelitian.
Selain itu, dari data studi klinik fase pertama yang dilakukan ditemukan adanya kejadian yang tidak diinginkan. Sebanyak 20 dari 28 subjek mengalami kejadian yang tidak diinginkan dalam tingkat 1 dan 2, seperti nyeri lokal, nyeri otot, nyeri sendi, nyeri kepala, penebalan, kemerahan, gatal, demam, batuk, pilek, lemas, dan mual.
Sementara itu, sebanyak enam subjek mengalami kejadian tidak diinginkan dalam tingkat 2, seperti hypernatremia (kadar natrium yang tinggi dalam darah), peningkat kadar ureum dalam darah (blood urea nitrogen), serta kolesterol.
“Kejadian yang tidak diinginkan grade 3 merupakan salah satu pada kriteria penghentian pelaksanaan uji klinik yang tercantum pada protokol uji klinik, namun berdasarkan informasi Tim Peneliti saat inspeksi yang dilakukan Badan POM, tidak dilakukan penghentian pelaksanaan uji klinik,” kata Penny.
Di lain sisi, ada tiga dari 28 subjek mengalami peningkatan titer antibodi empat kali lipat setelah 4 minggu penyuntikan sedangkan delapan dari 28 subjek mengalami penurunan antibodi. Dari dua subjek terdapat pada kelompok vaksin dengan kadar antigen 0,33 mcg (microgram) dan adjuvant 500 mcg serta satu subjek terdapat pada kelompok vaksin dengan kadar antigen 1,0 mcg dan adjuvant (tambahan) 500 mcg. Hal tersebut menunjukkan peningkatan kadar titer antibodi bisa dipengaruhi oleh peningkatan konsentrasi adjuvant, bukan karena peningkatan kadar antigen.
Penny menyampaikan, hal lain yang juga harus diperhatikan yaitu semua komponen utama pembuatan vaksin dendritik ini di Import dari AS, seperti antigen, GMCSF, medium pembuatan sel, dan alat-alat untuk persiapan. “Jika akan dilakukan transfer teknologi dan dibuat di Indonesia membutuhkan waktu yang lama karena sampai saat ini industri farmasi yang bekerjasama dengan Aivita Biomedica Inc belum memiliki sarana produksi untuk produk biologi dan membutuhkan waktu dua sampai lima tahun untuk mengembangkan di Indonesia,” kata Penny.
Kewaspadaan
Secara terpisah, Direktur Pencegahan dan Pengendalian Penyakit Menular Langsung Kementerian Kesehatan Siti Nadia Tarmizi mengatakan, kewaspadaan pada penularan Covid-19 harus terus ditingkatkan. Ini terutama setelah sejumlah negara menyatakan adanya peningkatan penularan.
Menurut dia, penularan yang tinggi terjadi karena mobilitas yang tinggi serta munculnya varian mutasi baru dari virus penyebab Covid-19 yang memiliki tingkat penularan yang lebih tinggi. Disiplin untuk melakukan protokol kesehatan merupakan hal penting yang harus terus dilakukan.
“Masyarakat diharapkan mematuhi larangan mudik agar tidak ada lonjakan kasus di Indonesia. Pemerintah kini juga terus memperkuat pengendalian penularan di pintu masuk negara, apalagi menjelang lebaran akan banyak PMI (pekerja migran Indonesia) yang pulang,” tutur Nadia.
Oleh DEONISIA ARLINTA
Editor: ICHWAN SUSANTO
Sumber: Kompas, 15 April 2021