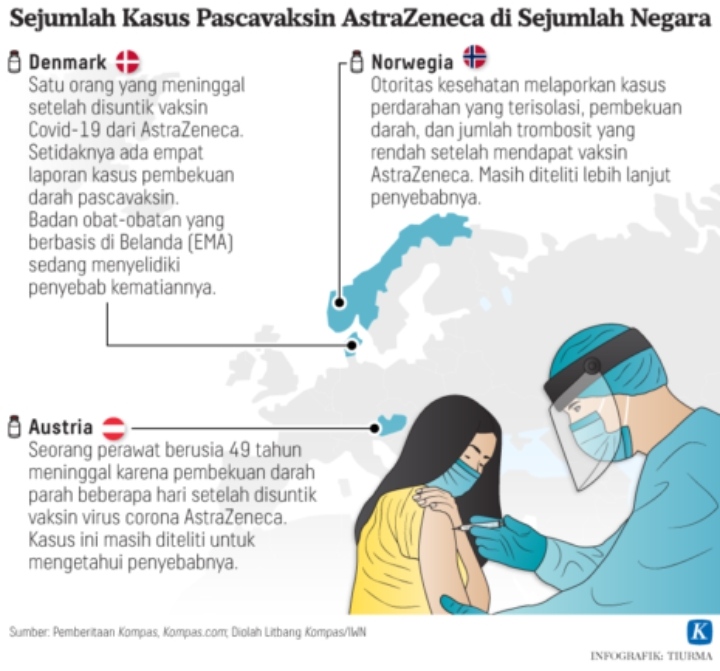
Pelaksanaan uji klinik vaksin Nusantara mesti dipantau Badan Pengawas Obat dan Makanan. Hal itu bertujuan untuk memastikan kandidat vaksin Covid-19 yang dikembangkan itu aman, manjur, dan efektif.
Di tengah pro-kontra yang muncul dari pengembangan vaksin Nusantara, basis sains harus tetap diutamakan. Penelitian yang dilakukan harus memastikan vaksin aman, bermutu, dan efektif untuk digunakan. Koordinasi antara Badan Pengawas Obat dan Makanan dan tim peneliti vaksin Nusantara pun dinilai perlu diperbaiki.
Ketua Tim Pakar sekaligus Juru Bicara Satuan Tugas Penanganan Covid-19 Wiku Adisasmito di Jakarta, Kamis (15/4/2021) mengatakan, vaksin Nusantara atau vaksin dendritik merupakan jenis vaksin yang dikembangkan di Amerika Serikat (AS) dan diuji coba di Indonesia. Pemerintah memberikan dukungan pada pengembangan seluruh vaksin, termasuk vaksin Nusantara selama vaksin tersebut memenuhi kriteria yang ditentukan.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
“Pada prinsipnya semua vaksin yang akan diberikan ke masyarakat harus mendapat izin dari Badan POM (Pengawas Obat dan Makanan), terutama terkait aspek keamanan, efikasi, dan kelayakan,” tambahnya. Tim pengembangan vaksin Nusantara diharapkan dapat berkoordinasi lebih baik dengan Badan POM agar isu yang ada terkait vaksin ini bisa segera diselesaikan.
Vaksin Nusantara dikembangkan oleh tim peneliti dari Badan Penelitian dan Pengembangan Kesehatan (Balitbangkes) Kementerian Kesehatan, Rumah Sakit Pusat Angkatan Darat (RSPAD) Gatot Subroto, Rumah Sakit Umum Pusat (RSUP) Dr Kariadi Semarang, dan Universitas Diponegoro. Penelitian ini disponsori oleh PT Rama Emerald atau PT Aivita Indonesia yang bekerja sama dengan Balitbangkes.
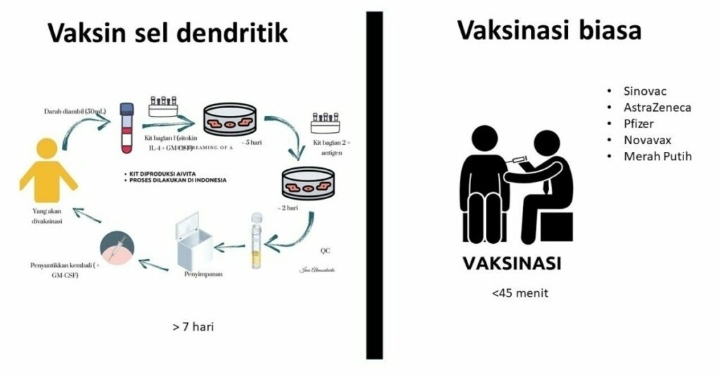
Vaksin tersebut merupakan vaksin yang menggunakan campuran dari sel dendritik yang berasal dari setiap orang yang menjadi sasaran vaksinasi, antigen SARS-CoV-2 spike protein (protein paku), dan GMCSF (sarmogastrim) yang menjadi faktor pertumbuhan. Antigen dan GMCSF saat ini belum diproduksi di Indonesia sehingga masih perlu diimpor dari AS.
Kepala Badan POM Penny K Lukito sebelumnya mengatakan, para peneliti vaksin Nusantara belum berkoordinasi dengan Badan POM mengenai pelaksanaan uji klinis tahap kedua. Bahkan, Badan POM justru meminta para peneliti untuk kembali melakukan uji preklinik karena data yang didiserahkan peneliti masih belum memadai.
Adapun hasil pengujian yang belum memadai itu, meliputi keamanan vaksin, kemampuan vaksin dalam membentuk antibodi, serta bukti mutu produk vaksin. Selain itu, dari hasil inspeksi yang dilakukan Badan POM, pengembangan vaksin tersebut juga belum sesuai dengan kaidah cara produksi yang baik (good manufacturing practices/GMP), cara berlabolatorium yang baik (good laboratory practice/GLP), dan cara uji klinik yang baik (good clinical practice/GCP).
 Dalam inspeksi tersebut ditemukan sejumlah hal yang tidak sesuai kaidah antara lain, produk vaksin dibuat dalam kondisi tidak steril, metode pengujian tidak dilakukan validasi dan standardisasi, serta adanya inkonsistensi pencatatan data. Subjek yang seharusnya tidak masuk dalam kriteria inklusi, seperti sudah memiliki antibodi, tetap diikutkan dalam penelitian.
Dalam inspeksi tersebut ditemukan sejumlah hal yang tidak sesuai kaidah antara lain, produk vaksin dibuat dalam kondisi tidak steril, metode pengujian tidak dilakukan validasi dan standardisasi, serta adanya inkonsistensi pencatatan data. Subjek yang seharusnya tidak masuk dalam kriteria inklusi, seperti sudah memiliki antibodi, tetap diikutkan dalam penelitian.
Hal lain yang juga mendapatkan perhatian yakni ada temuan kejadian yang tidak diinginkan dari subyek dalam uji klinik tahap pertama. Sebanyak 20 dari 28 subjek pengujian atau sebesar 71,4 persen mengalami kejadian tidak diinginkan dalam tingkat 1 dan 2, seperti nyeri lokal, nyeri otot, nyeri sendi, nyeri kepala, kemerahan, gatal, demam, batuk, pilek, lemas, dan mual.
Sementara itu, sebanyak enam subyek riset mengalami kejadian tidak diinginkan tingkat 3, seperti hypernatremia (kadar natrium yang tinggi dalam darah), peningkatan kadar ureum dalam darah (blood urea nitrogen), serta kolesterol.
” Kejadian yang tidak diinginkan grade 3 merupakan salah satu pada kriteria penghentian pelaksanaan uji klinik yang tercantum pada protokol uji klinik, tetapi berdasarkan informasi tim peneliti saat inspeksi yang dilakukan Badan POM, tidak dilakukan penghentian pelaksanaan uji klinik,” kata Penny.
Data yang diterima Badan POM juga menyebutkan, semua komponen utama pembuatan vaksin dendritik ini diimpor dari AS, seperti antigen, GMCSF, medium pembuatan sel, dan alat-alat untuk persiapan.
” Jika akan dilakukan transfer teknologi dan dibuat di Indonesia, maka membutuhkan waktu lama. Sebab, sampai saat ini industri farmasi yang bekerja sama dengan Aivita Biomedica Inc belum memiliki sarana produksi untuk produk biologi dan membutuhkan waktu dua sampai lima tahun untuk mengembangkan di Indonesia,” tutur Penny.
Oleh DEONISIA ARLINTA
Editor: EVY RACHMAWATI
Sumber: Kompas, 16 April 2021