Ada ilmuwan yang mencapai ketenaran segera setelah ia menemukan sesuatu pada cabang ilmunya itu. Ada pula ilmuwan yang menemukan ketenaran itu baru di kemudian hari, pada hari tuanya. Namun, ada juga ilmuwan yang meraih ketenaran justru setelah ia meninggal dunia. Amedeo Avogadro, bangsawan Quaregna, termasuk salah seorang ilmuwan pada golongan terakhir ini. Hipotesisnya baru diakui di kalangan ilmuwan, tak lama setelah ia meninggal, atau setengah abad setelah hipotesis itu dikemukakan.
Kini, salah satu bilangan di bidang ilmu alam telah diberi nama bilangan Avogadro. Dan bersama itu, Avogadro terkenal sampai ke kalangan pelajar di seluruh dunia. Secara lebih terperinci, bilangan Avogadro adalah banyaknya atom atau molekul di dalam satu gramatom atau gramolekul zat. Sekalipun nilai bilangan ini bukan berasal dari Avogadro, namun bilangan itu berkaitan dengan hipotesis yang dikemukakannya pada tahun 1811.
Berat Lawan Isi
Pada tahun 1802, Joseph Louis Gay Lussac mengumumkan, bahwa pada suatu kenaikan temperatur tertentu, semua gas memuai dengan ukuran yang sama. Hukum ini dikenal sebagai hukum Gay-Lussac. Sesungguhnya, hal ini sudah terlebih dahulu ditemukan oleh Jacques Alexandre Cesar Charles. Namun, Charles tidak mengumumkan penemuannya, sehingga banyak orang menganggap bahwa Gay-Lussac sebagai penemunya. Sekalipun demikian, masih saja ada orang yang mengingat jasa Charles. Tidak heran, kalau di beberapa buku, hukum ini juga dikenal sebagai hukum Charles.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
Pada tahun 1803, John Dalton mengumumkan hukum proporsi ganda: hukum yang menyatakan bahwa unsur dapat bergabung menurut proporsi berat yang merupakan bilangan bulat sederhana. Air, misalnya, terdiri atas gabungan satu bagian berat hidrogen terhadap 8 bagian berat oksigen.
Pada tahun 1809, dengan bantuan Friedrich Wilhelm Heinrich von Humboldt, Gay-Lussac menemukan bahwa dalam pembentukan zat gabungan, gas bergabung menurut proporsi isi yang dapat dinyatakan dengan bilangan bulat sederhana. Uap air, misalnya, terdiri atas gabungan dua bagian isi hidrogen terhadap satu bagian isi oksigen.
Dalton tidak menyetujui pernyataan Gay-Lussac tapi tetap berpegang kepada proporsi berat. Sejak itu, terjadilah pertentangan di dalam proporsi penggabungan zat. Dalam hal air, yang merupakan gabungan dari hidrogen dan oksigen saja, misalnya, hukum mana yang harus kita turuti: proporsi berat ataukah proporsi isi? Sampai di sini, muncullah Avogadro dengan hipotesisnya.
Hipotesis Avogadro
Mula-mula, Avogadro mempelajari hukum. Pada tahun 1796, ia lulus sebagai doktor di bidang hukum, dan praktek di bidang itu selama tiga tahun. Namun, Avogadro kemudian tertarik kepada ilmu alam. Bahkan, pada usia tuanya, ia menjadi guru besar fisika di Universitas Turin.
 Mendengar hukum Gay-Lussac yang menyatakan bahwa pada suatu kenaikan temperatur tertentu, semua gas akan memuai dengan ukuran yang sama, maka ia pun mulai berpikir. Pada tahun 1811, hasil pemikiran itu ditulisnya di dalam satu makalah. Ka.lau semua gas bertindak sama pada kenaikan temperatur seperti yang dikatakan Gay-Lussac, pikir Avogadro, maka pada suatu temperatur tertentu, semua gas seharusnya memiliki jumlah partikel yang sama per satuan isi.
Mendengar hukum Gay-Lussac yang menyatakan bahwa pada suatu kenaikan temperatur tertentu, semua gas akan memuai dengan ukuran yang sama, maka ia pun mulai berpikir. Pada tahun 1811, hasil pemikiran itu ditulisnya di dalam satu makalah. Ka.lau semua gas bertindak sama pada kenaikan temperatur seperti yang dikatakan Gay-Lussac, pikir Avogadro, maka pada suatu temperatur tertentu, semua gas seharusnya memiliki jumlah partikel yang sama per satuan isi.
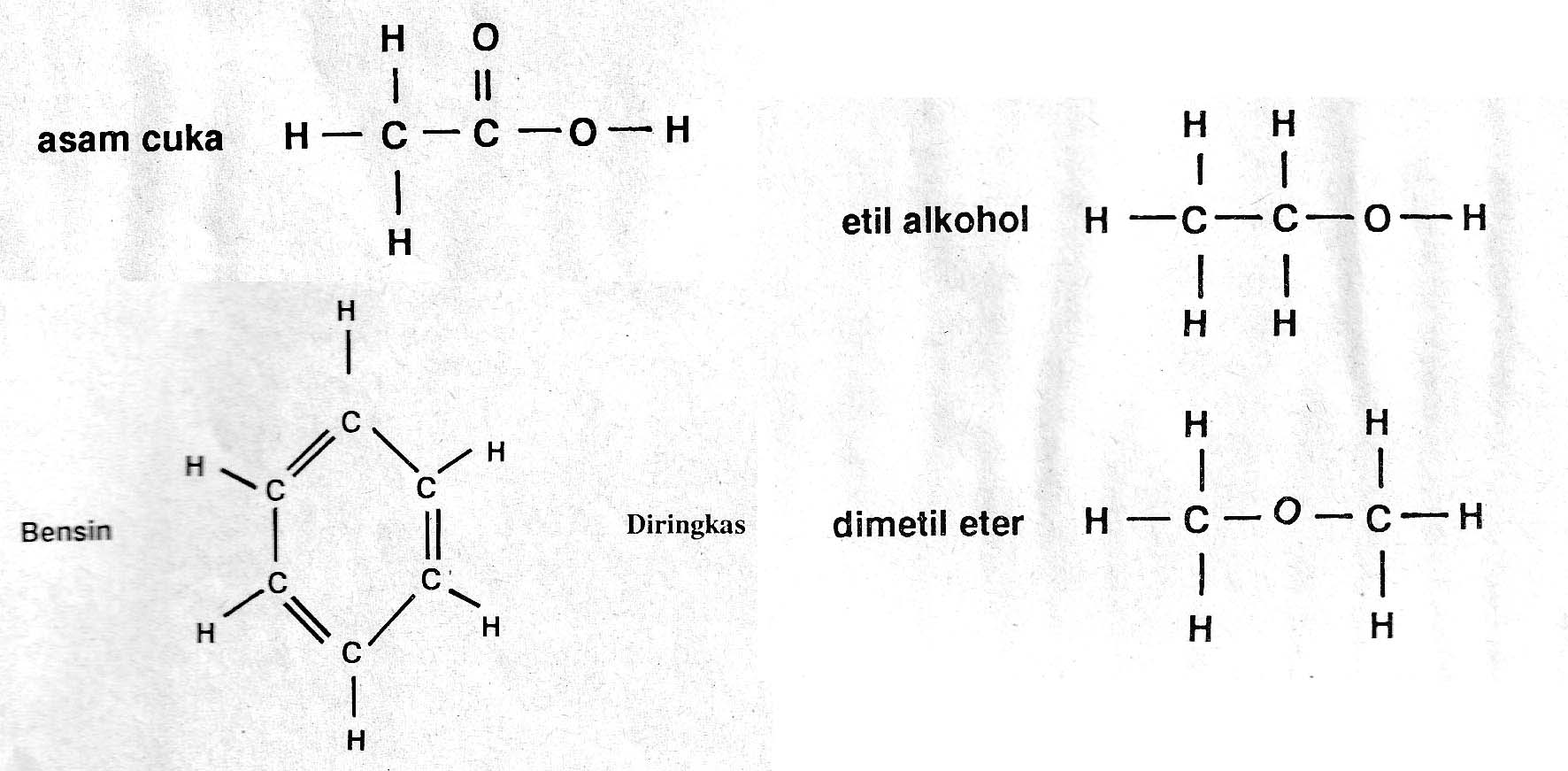
Di dalam hipotesisnya itu, Avogadro cukup berhati-hati. Ia berpendapat, bahwa partikel itu tidak harus berbentuk atom. Ada kemungkinan bahwa partikel itu terdiri atas gabungan atom yang dinamakan molekul. Dengan demikian, Avogadro merupakan orang pertama yang membedakan atom dengan molekul.
Dengan hipotesis ini, Avogadro dapat menjelaskan hukum Gay-Lussac. Apalagi pada awal abad itu, melalui elektrolisis, Johann Wilhelm Ritter telah berhasil memisahkan air ke dalam hidrogen dan oksigen. Isi hidrogen dan oksigen hasil elektrolisis ini berbanding dua terhadap satu. Melalui hipotesisnya, Avogadro menyatakan, bahwa molekul air terdiri atas dua atom hidrogen dan satu atom oksigen.
Selanjutnya, kalau Dalton mengatakan bahwa berat oksigen dalam air adalah delapan kali berat hidrogen, maka menurut Avogadro, perbandingan berat itu adalah terhadap dua atom hidrogen. Jadi, berat satu atorn oksigen terhadap dua atom hidrogen, adalah delapan kali. Dengan demikian, pethandingan berat satu atom oksigen terhadap satu atom hidrogen seharusnya adalah 16, bukan 8.
Kongres Kimia Internasional
Ternyata,hipotesis Avogadro ini ditentang para ilmuwan terkenal masa itu. Secara gigih, Dalton tak mau mengakui hipotesis Avogadro. Jons Jacob Berzelius, ahli kimia terkenal zaman itu, juga mengabaikannya. Dan pengabaian ini bukannya tanpa akibat.
Terjadilah kekacauan dalam pengertian atom dan molekul. Demikian pula, terjadi kekacauan dalam pengertian berat atom dan berat molekul. Rumus untuk struktur zat dalam bentuk molekul serta atom yang membentuk molekul itu menjadi simpang siur. Tidak ada persesuaian paham tentang berat atom pada sejumlah unsur. Akibatnya, zat sederhana seperti asam asetat memiliki sampai sebanyak 19 macam rumus yang diberikan oleh berbagai ahli kimia.
Dalam keputusasaan, Friedrich August Kekule von Stradonitz mengusulkan untuk diadakan suatu konperensi yang dihadiri oleh ahli kimia se-Eropa untuk membahas hal ini. Bersama itu, untuk pertamakalinya dalam sejarah, pertemuan intemasional ilmiah diadakan pada tahun 1860, di kota Karlsruhe, kerajaan Baden. Pertemuan itu dinamakan Kongres Kimia Internasional pertama.
Di samping Kekule, hadir pula para ahli kimia lain seperti Wohler, Liebig, Bunsen, Mendeleev, dan lain-lainnya. Juga hadir Stanislao Cannizzaro. Sebelumnya, pada tahun 1858, ia telah membaca hipotesis Avogadro, serta melihat bahwa hipotesis itu dapat menyelesaikan kemelut yang dihadapi para ahli kimia. Dengan bekal hipotesis Avogadro, ia menyusun suatu makalah tentang itu, dan datang ke kongres.
Dengan semangat yang berapi-api, serta pidato yang berkobar-kobar, ia memperkenalkan lagi hipotesis Avo-gadro. Ia menjelaskan bagaimana hipotesis itu dapat digunakan untuk membedakan atom dan molekul. Dan, setelah kongres usai, semakin banyak ahli kimia yang berhasil diyakininya. Bersama itu, secara mantap, para ahli kimia bergerak menuju ke kesesuaian penuh dalam rumusan kimia dari hampir semua zat sederhana.
Para ilmuwan akhirnya menerima Avogadro , dan Avogadro pun terkenal. Namun, Avogadro sendiri tidak pemah menikmati ketenarannya itu. Avogadro telah meninggal beberapa tahun sebelum konares itu diselenggarakan. Yah, menyedihkan, memang. Tapi, begitulah sejarah manusia.
Bilangan Avogadro
Sebenarnya, Avogadro hanya mengatakan bahwa pada suatu temperatur tertentu, per satuan isi, semua gas mengandung partikel yang sama banyaknya. Tapi, kemudian, para ilmuwan menemukan bahwa satu gramatom atau gramolekul zat juga mengandung atom atau molekul yang sama banyaknya. Banyaknya atom atau molekul ini adalah sama dengan banyaknya partikel yang dikemukakan oleh Avogadro. Dan banyaknya partikel, atom, atau molekul ini, kini, dikenal sebagai bilangan Avogadro.
Tidak ada orang yang dapat mengetahui secara tepat berapa besar bilangan Avogadro itu. Perhitungan yang ada hanyalah bilangan yang dibulatkan sampai ke ketelitian jutajutaan. Namun, melalui perkembangan pengetahuan di bidang fisika, kini, bilangan ini dapat dihitung dengan cara tak langsung. Hasil perhitungan menunjukkan bahwa bilangan Avogadro adalah
602 .600.000 .000 .000.000 .000.000 molekul/gramolekul
Ada beberapa cara untuk menentukan nilai ini. Perrin, misalnya, menggunakan cara suspensi koloid untuk menentukan bilangan Avogadro. Butir mikroskopic dari suatu zat damar disuspensikan ke dalam cairan yang mempunyai densitas (kerapatan) yang sedikit lebih rendah. Waktu butiran itu melayang di dalam cairan, Perrin menggunakan mikroskop untuk menentukan konsentrasi butiran itu sebagai fungsi kedalaman. Dengan cara ini, Perrin menemukan nilai bilangan Avogadro.
Cara lain adalah melalui elektrolisis. Dengan mengetahui muatan elektron, konstanta Faraday, serta endapan zat univalent seperti perak, bilangan Avogadro ini dapat dihitung.
Dengan munculnya pengetahuan di bidang sinar X dan radioaktivitas, bilangan Avogadro pun dapat dihitung melalui cara sinar X atau cara radioaktivitas.
Di samping cara ini, masih terdapat sejumlah cara lain untuk menentukan bilangan Avogadro setepat mungkin. Namun, berapa pun nilai bilangan itu, Avogadro ternyata benar ketika ia mengemukakan: bahwa pada keadaan tertentu, banyaknya partikel, baik atom maupun molekul, adalah sama untuk isi yang sama.
Oleh Dali S. Naga
Sumber: Majalah AKU TAHU/ Januari 1985