Vaksin adalah domai kedokteran dan kesehatan. Maka biarkanlah orang-orang profesional di bidang ini yang menjadi penentu. Tidak perlu diintervensi. Pihak peneliti dan BPOM perlu berkomunikasi intens satu meja.
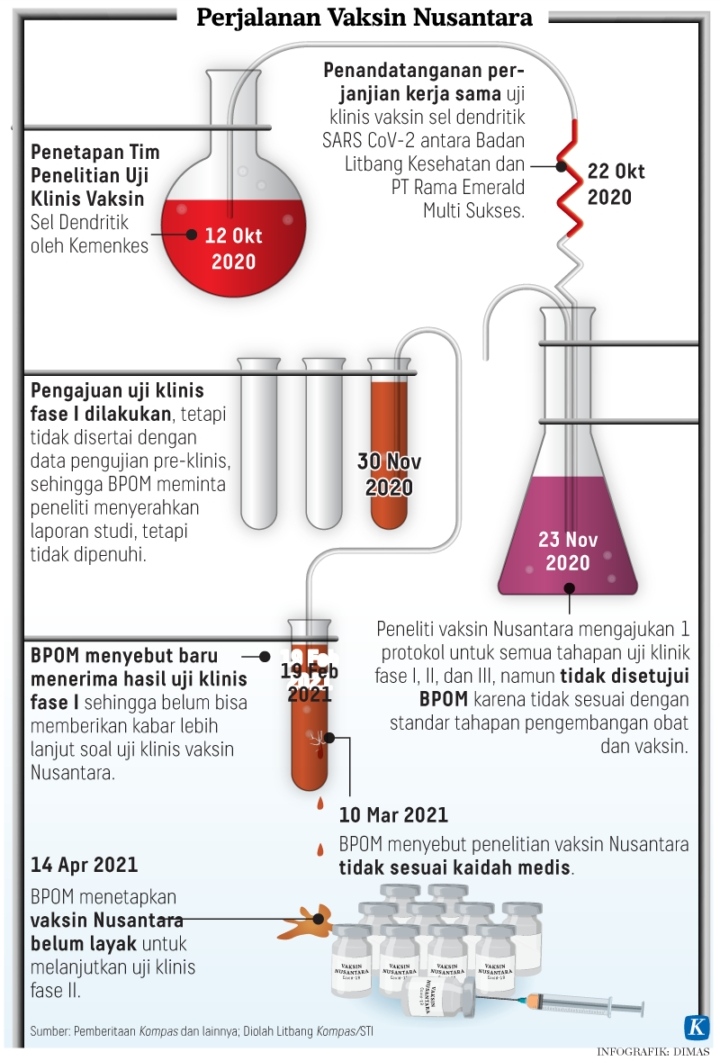
Vaksin Nusantara tiba-tiba menjadi isu kontroversial. Awalnya sederhana. Mantan Menteri Kesehatan Agus Terawan dan timnya mengadakan uji coba vaksin Covid-19 berbasis sel dendritik di Indonesia. Saat ini, uji coba telah masuk tahap 2 dan dilakukan pada sejumlah terbatas subyek. Sejumlah pihak mengklaim vaksin ini karya anak bangsa.
Mungkin karena namanya vaksin Nusantara. Antara lain karena alasan ini, sejumlah pihak mendukung penuh, termasuk beberapa tokoh publik. Berita dukungan mereka tersebar ke media massa dan media sosial. Beberapa anggota DPR ikut berpartisipasi sebagai subyek uji coba. Alasannya, nasionalisme; produk anak bangsa harus didukung maksimal. Dukungan mengalir.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
Di sisi lain, BPOM sebagai regulatory body bahan obat dan makanan di Indonesia tidak atau belum memberi izin melanjutkan penelitian. Alasannya tegas; hingga saat ini penelitian ini tak memenuhi standar pengujian vaksin yang tepat dan baik.
BPOM pun jadi bulan-bulanan sebagian pihak. Dianggap tidak nasionalis. Tidak mendukung karya anak bangsa.
“Dendritic-based vaccine”
Secara sederhana sel dendritik adalah sel dalam tubuh manusia yang dapat menginduksi, mengoordinasi dan mengatur respons imun. Karenanya, dinamakan juga antigen presenting cell. Sel ini terdapat pada kulit, hidung, paru-paru dan darah. Secara fungsional, sel dendritik dikategorikan atas dua jenis, yaitu yang mature dan immature.
Sel immature berfungsi mengambil dan memproses antigen yang masuk ke tubuh. Sedangkan sel mature berfungsi mempresentasikan antigen. Dengan kerja sel dendritik ini, tubuh mengidentifikasi dan meregulasi antigen dan selanjutnya merangsang timbulnya antibodi, termasuk limfosit T.
 Selain itu, respons imun yang dibentuk dapat mencakup Th1, Th2, Treg atau Th17. Mengutak-atik sel dendritik diharapkan dapat membangun respons imun dan antibodi. Dan prinsip ini yang menjadi basis studi vaksin Nusantara.
Selain itu, respons imun yang dibentuk dapat mencakup Th1, Th2, Treg atau Th17. Mengutak-atik sel dendritik diharapkan dapat membangun respons imun dan antibodi. Dan prinsip ini yang menjadi basis studi vaksin Nusantara.
Sel dendritik sejatinya bukan isu baru di dunia kedokteran. Ralph Steinmann dan Zanvil Cohn dari Universitas Rockefeller pada 1973 pertama kali menemukan adanya sel yang bentuk dan gerakannya aneh pada limpa tikus. Sel ini menyerupai pohon, karenanya dinamakan sel dendritik. Dalam bahasa Yunani, dendritik berarti pohon.
Pada manusia, Paul Langerhans yang pertama kali mengidentifikasi sel ini pada kulit manusia. Sebelum ditemukannya sel dendritik, penelitian imunologis penyakit lebih banyak terfokus pada antigen dan limfosit. Setelah penemuan bersejarah ini, sel dendritik menjadi alternatif obyek studi. Banyak penelitian yang mempelajari peranan sel dendritik terhadap penyakit, terutama kanker dan infeksi. Salah satu di antaranya adalah studi vaksinasi kanker.
Penelitian ini mempelajari bagaimana menggunakan respons imunitas, terutama sel dendritik, dalam mengobati kanker. Sel dendritik, baik secara tunggal maupun kombinasi dengan obat kanker lainnya, dihipotesiskan dapat menghentikan laju penyakit kanker. Namun studi-studi pada berbagai jenis kanker ini belum memberikan hasil yang meyakinkan. Sebagian dianggap berpotensi bermanfaat dan sebagian lagi tidak bermanfaat. Kasarnya, belum memuaskan.
Diilhami hipotesis peranan sel dendritik dalam meningkatkan antibodi, beberapa ahli kemudian melakukan ekstrapolasi hipotesis. Bahwa sel dendritik juga bisa bermanfaat sebagai vaksin Covid-19. Hipotesis ini muncul sejalan dengan merebaknya pandemi.
Sejumlah penelitian mempelajari pembuatan vaksin Covid-19 dengan menggunakan sel dendritik. Salah satu pionernya Celartics Biopharma di China. Pada 20 Mei 2020, perusahaan ini diberitakan telah mematenkan vaksin mereka yang memakai sel dendritik, yang dinamai Cov-DCVax.
Namun berita perkembangan vaksin ini menjadi tak jelas saat ini. Selain Celartics, perusahaan AS, Aivita Biomedical juga meneliti pembuatan vaksin Covid-19 dengan sel dendritik.
Karya anak bangsa?
Potensi vaksin yang sementara diteliti oleh tim Terawan tercatat di US Clinical Trial Government. Meski demikian, disclaimer pencatatan ini menyatakan bahwa ketercantuman dalam daftar ini bukan berarti bahwa penelitian ini telah disetujui pemerintah AS atau US Federal Government. Penelitian ini juga tercatat di Kementerian Kesehatan RI. Meski tercatat, nama vaksin yang diteliti bukan vaksin Nusantara tetapi Cov-DCVax. Entah nama Nusantara muncul dari mana.
Pada kedua registrasi itu disebutkan bahwa kolaborator vaksin ini adalah Aivita Biomedical Inc Amerika, PT Aivita Biomedikal Indonesia, Kementerian Kesehatan RI, RSUP Kariadi Semarang dan Fakultas Kedokteran Universitas Diponegoro. Jadi penelitian ini legal. Bukan kucing-kucingan. Aivita Biomedical sendiri adalah sebuah perusahan Amerika yang fokus dalam pembuatan vaksin untuk kanker dan Covid-19.
Dalam situs mereka disebutkan, vaksin yang diujicobakan di Indonesia adalah buatan mereka. Proyek mereka. Vaksin mereka ini menggunakan sel dendritik autologous yang telah diisi spike protein Covid-19. Uji coba dilakukan di Indonesia. Mereka sementara menjajaki kemungkinan melakukan uji serupa di AS.
Jadi konsep vaksin, bahan, alatnya dan sebagian peneliti yang terlibat dalam vaksin ini berasal dari perusahaan AS ini. Indonesia hanya jadi tempat uji coba. Maka terdengar aneh bila vaksin ini dianggap karya anak bangsa. Apalagi dihubungkan dengan nasionalisme.
Dalam rilis informasi per 25 Februari, Aivita mengklaim mereka telah sukses menyelesaikan fase 1 uji vaksinnya di Indonesia. Uji tahap 1 ini memakan waktu lebih dari sebulan. Dengan menggunakan 27 orang coba, mereka menyebutkan hasil uji klinik tahap 1 berjalan baik, bisa ditoleransi, tak menimbulkan efek samping serius dan orang yang menjalani uji coba terbukti telah memproduksi antibodi. Mereka merencanakan uji vaksin ini akan berlangsung setahun, hingga 31 Januari 2022.
Rilis ini tampaknya tak sesuai dengan catatan BPOM. BPOM awalnya telah memberikan izin pelaksanaan uji klinik fase 1 sambil terus melakukan pemonitoran dan pendampingan. Namun dalam perjalanannya, BPOM mencatat sejumlah hal ganjil terkait uji klinis ini. Karena itu, BPOM tidak atau belum memberikan izin untuk melanjutkan ke fase 2.
Dianggap belum layak masuk fase 2. Alasannya, penelitian tak penuhi berbagai syarat penting yang diperlukan, di antaranya cara uji klinik yang baik (good clinical practice), pembuktian konsep studi (proof of concept), praktik laboratorium yang baik (good laboratory practice) dan cara pembuatan bahan yang baik (good manufacturing practice).
Lebih dari itu, jenis bahan vaksin yang digunakan dianggap tak memenuhi derajat memuaskan dari bahan (pharmaceutical guide) dan karena itu tak memenuhi kriteria pembuktian konsep yang baik. BPOM juga mencatat beragam efek samping dan menganggap penelitian ini tak penuhi kaidah medis karena terkait persoalan komite medik.
“Evidence-based medicine”
Bidang kedokteran adalah bidang sains yang presisi. Bukan mengawang-awang. Semua hipotesis dan konsep yang digunakan atau dipraktikkan mesti diuji dan dikalibrasi dengan standar uji ketat, diakui dan terstandarisasi.
Memenuhi standar evidence-based medicine. Termasuk persetujuan penggunaan obat dan vaksin. Ini penting karena menyangkut hayat hidup orang banyak. Dapat memberi efek serius dan bahkan mematikan. Untuk persetujuan vaksin, keterpenuhan evidence-based medicine diukur dengan pelaksanaan uji vaksin yang terstandarisasi secara internasional. Standar ini universal; semua negara menganutnya. Fase uji vaksin standar terdiri atas fase pre-klinis (percobaan binatang) dan fase klinis (percobaan pada manusia).
Fase klinis terdiri atas 3 fase utama, yang tiap-tiap fase memiliki tujuan dan standar berbeda terkait tujuan, jumlah orang yang diuji, kriteria keamanan dan sebagainya. Fase-fase ini sangat ketat standarnya. Pada setiap fase ada indikator yang harus dipenuhi dan tak bisa ditawar-tawar.
Sebelum memberikan persetujuan uji dan penggunaan vaksin, regulatory body setiap negara wajib mempelajari, mengawasi dan memantau uji vaksin. Uji vaksin harus benar dan sesuai standar. Bila ada hal-hal yang tak bersesuaian atau bertentangan dengan kriteria standar, regulatory body berhak menegur, tak melanjutkan atau bahkan mencabut izin penelitian. Ini tugas dan domain mereka.
Sebagai regulatory body di Indonesia, BPOM tentu harus bekerja profesional. Menegakkan prinsip-prinsip evidence-based medicine dan standar sains yang berlaku. Prinsip ini absolut dan tidak bisa ditawar-tawar. Karena menyangkut hajat hidup orang banyak, tidak boleh neko-neko dan menoleransi praktik yang tidak bersesuaian demi kepentingan tertentu. Dan ini berlaku universal.
Semua obyek harus diperlakukan sama. Termasuk proyek vaksin Nusantara. Harus dikawal dan dievaluasi agar proses uji klinik yang dilakukan benar-benar memenuhi standar. Proses sama juga terjadi saat pengajuan persetujuan vaksin Sinovac sebelumnya. Persetujuan vaksin ini sempat tertunda beberapa waktu karena ada beberapa hal yang perlu diperjelas dan dilengkapi dari uji vaksin ini.
Nasionalisme versus sains?
Kalau dilihat secara utuh, sejatinya vaksin Nusantara ini bukan karya anak bangsa. Ini adalah proyek yang dilahirkan dan dikembangkan oleh perusahaan vaksin AS, Aivita. Mulai dari konsep, hipotesis, bahan dan alatnya, punya mereka. Sebagian peneliti juga adalah orang mereka. Ini proyek mereka. Indonesia hanya menjadi tempat uji coba penelitian ini. Plus iming-iming transfer teknologi tentunya.
Jadi secara kasar, proyek vaksin ini tak beda dengan vaksin Sinovac. Konsep, bahan dan kits-nya semua dari China. Indonesia jadi tempat uji coba. Kalaupun kita mengotot mencari perbedaan, maka perbedaannya hanya terletak pada bahan yang digunakan.
Vaksin Sinovac menggunakan kuman Covid-19 yang dimatikan, sedangkan vaksin Nusantara menggunakan sel dendritik. Dengan kondisi demikian, terlalu berlebihan bila vaksin ini digembar-gemborkan sebagai karya anak bangsa. Apalagi sampai menghubung-hubungkan semangat nasionalisme dengan vaksin ini.
Sel dendritik sendiri bukan barang gaib atau imajinasi. Ini sebuah konsep medis modern yang sementara berkembang dan sementara banyak diteliti. Ini saintifik. Jadi wajar bila ada pihak-pihak tertentu yang ingin mempelajari dan menggali lebih dalam konsep ini, termasuk dalam bidang vaksin Covid-19.
Tak ada yang keliru. Yang perlu dipahami, penelitian sel dendritik vaksin Covid-19 ini masih penelitian tahap awal. Konsepnya masih berupa hipotesis yang masih harus dibuktikan. Bisa saja nanti terbukti bahwa sel dendritik ini jadi bahan vaksin Covid-19 yang hebat dan berguna. Bisa juga sebaliknya.
Hanya uji vaksin yang ilmiah dan standarlah yang mampu membuktikan apakah sel dendritik vaksin ini nanti bermanfaat atau tak berguna (useless). Tak ada cara lain. Karena itu, tim peneliti sudah selayaknya menghargai, memenuhi dan menjalankan standar dan protokol uji vaksin yang benar. Termasuk memerhatikan dan memenuhi catatan atau rekomendasi BPOM. Bukan melanjutkan penelitian sesuai keinginan.
Pihak peneliti dan BPOM mesti duduk satu meja. Melakukan komunikasi lebih intens dan profesional. Melihat celah untuk membuat penelitian lebih baik dan bermanfaat. Sejumlah tokoh publik perlu menahan diri untuk tak berpihak. Apalagi memberi image prematur bahwa vaksin ini baik, sukses dan bermanfaat. Padahal vaksin ini sendiri masih dalam taraf awal penelitian dan ujung penelitiannya masih setahun lagi.
Semua bidang memiliki domain spesifik. Vaksin adalah domain kedokteran dan kesehatan. Maka biarkanlah orang-orang profesional di bidang ini yang menjadi penentu. Tidak perlu diintervensi. Mungkin masih ingat sebuah pesan : bila engkau menyerahkan sebuah urusan kepada orang yang bukan ahlinya, maka tunggulah kehancuran.
Iqbal Mochtar Dokter dan Pengamat Masalah Kesehatan
Editor: YOHANES KRISNAWAN
Sumber: Kompas, 19 April 2021