PENYAKIT mad cow yang banyak diberitakan di media massa akhir-akhir ini digolongkan sebagai penyakit yang misterius. Misterius karena penyakit itu disebabkan oleh suatu protein tanpa asam nukleat, yang disebut prion. Sampai saat ini belum diketahui dengan jelas bagaimana protein itu dapat memperbanyak diri tanpa melibatkan bahan genetik konvensional asam nukleat DNA atau RNA.
Prion
Bovine Spongiform Encephalopathy (BSE), yang umum disebut mad cow merupakan salah satu jenis penyakit scrapie pada hewan. Pada manusia, penyakit yang sejenis BSE itu dikenal ada empat macam, yaitu: penyakit kuru, Creutzfeldt-Jakob Disease (CJD), Gerstmann-Straussler-Scheinker Disease (GSS), dan, Fatal Familial Insomnia (FFI).
Penyakit scrapie pada mulanya diperkirakan disebabkan suatu parasit yang disebut Sarcosporidia. Penelitian lebih lanjut menunjukkan bahwa partikel scrapie dapat menembus filter bakteri, sehingga hipotesis mengenai virus yang terfiltrasi menjadi populer.
ADVERTISEMENT
SCROLL TO RESUME CONTENT
Meskipun demikian, partikel scrapie ini resisten terhadap inaktivasi oleh radiasi ultraviolet pada panjang gelombang 254 nm yang biasanya dapat menghancurkan DNA atau RNA.
Selain itu, berbagai usaha pemurnian tidak berhasil membuktikan adanya molekul asam nukleat spesifik untuk partikel scrapie. Sebaliknya, perlakuanpcrlakuan yang dapat memodifikasi atau menghancurkan protein dapat melenyapkan sifat infeksi partikel scrapie
Oleh karena itu partikel scrapie tidak dapat digolongkan sebagai virus konvensional ataupun viroid. Virus merupakan agen infeksi yang membawa DNA atau RNA di dalam selubung protein, sedangkan sebagian besar viroid yang menginfeksi tumbuhan pada dasarnya hanya berupa asam nukleat bugil.
Penelitian-penelitian yang lebih rinci sekitar tiga dasawarsa yang lalu memperlihatkan bukti-bukti bahwa partikel sciapie hanyalah suatu molekul protein tanpa asam nukleat.
Karena itu, diusulkan suatu konsep baru mengenai molekul protein yang dapat memperbanyak diri dan bersifat menular, yang disebut prion. Istilah prion diperkenalkan untuk membedakan protein infektif yang menyebabkan scrapie (termasuk penyakit mad cow), kuru CJD, GSS, dan FFI dari virus atau viroid.
Penemuan Prion
Setelah diketahui bahwa infektivitas scrapie tergantung pada protein, maka penelitian-penelitian yang bertujuan mencari protein-protein yang spesifik pada scrapie menjadi sangat intensif. Meskipun sifat tidak larut air dari protein scrapie menyulitkan proses pemurniannya tetapi sifatnya yang relatif tahan terhadap berbagai jenis protease sangat membantu dalam meningkatkan derajad kemurniannya.
Protein prion, biasa disingkat PrP, dapat diperoleh dari jaringan otak hewan yang terserang scrapie. Bagian dari prion yang resisten terhadap degradasi proteolitik berbobot molekul 27-30 kDa sehingga dikenal sebagai PrP27-30.
PrP27-30 ini ternyata merupakan basil pemrosesan molekul protein yang lebih besar (bobot molekul. 33-35 kDa) yang disebut PrPsc (protein prion scrapie).
Pada saat yang sama juga dilaporkan bahwa otak normal atau pun otak yang terserang scrapie mengekspresikan prion yang sensitif pada protease (disebut PrPc) dalam jumlah yang sama.
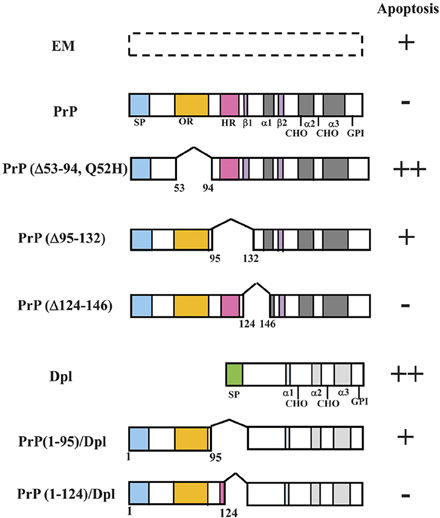
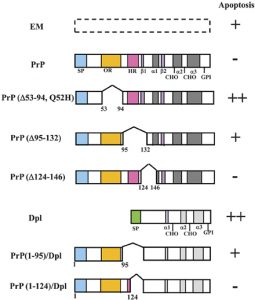
Selanjutnya diketahui bahwa protein prion yang infektif, yaitu PrPsc, merupakan isomorf (dua atau lebih molekul protein dengan sekuen asam amino yang identik tetapi berbeda konformasinya) dari PrPc.
PrPc disandikan oleh gen pada hewan dan manusia. Pada manusia, gen-gen PrP telah dipetakan pada lengan pendek kromosom nomor 20. Seluruh kerangka baca terbuka (open reading frame) dari gen PrP pada manusia atau burung terdapat pada satu ekson tunggal. Pada Syrian hamster, gen PrP dipisahkan oleh sebuah intron sepanjang 10 kb.
Perbanyak diri?
 Telah bertahun-tahun lamanya kasus CJD pada orang Yahudi asal Libya diperkirakan karena kebiasaan memakan otak dan bola mata domba yang dimasak setengah matang. Hal itu menunjukkan faktor transmisi atau sifat menular dari partikel penyebab CJD.
Telah bertahun-tahun lamanya kasus CJD pada orang Yahudi asal Libya diperkirakan karena kebiasaan memakan otak dan bola mata domba yang dimasak setengah matang. Hal itu menunjukkan faktor transmisi atau sifat menular dari partikel penyebab CJD.
Aspek transmisi atau penularan CJD pada manusia dapat terjadi antan lain karena transplantasi kornea, atau karena peralatan pembedahan yang tercemar. Beberap laporan menunjukkan bahwa kornea binatang yang terinfeksi mengandung prion dalam jumlah besar. Selain itu, CJD juga sangat mungkin menular karena pemakaian hormon tumbuh manusia, yang biasanya diekstrak dari kelenjar pituari mayat manusia.
Meskipun demikian, beberapa penelitian yang lain menunjukkan bahwa CJD pada beberapa keluarga Yahudi di Libya dan Tunisia berkaitan dengan adanya mutasi pada gen penyandi PrP, sehingga dalam hal ini ada kaitan genetik.
Mutasi itu adalah mutasi titik E200K pada gen PrP sehingga residu glutamat berubah menjadi lisin pada posisi asam amino yang ke 200 dari protein PrP. Mutasi E200K pada PrP juga ditemukan pada beberapa keluarga dari kelompok etnis yang lain.
Selain itu, manifestasi CJD juga berkaitan dengan mutasi D178N, dimana residu aspartat berubah menjadi asparagin pada posisi asam amino ke 178. Mutasi ini mengubah molekul PrPc (isomorf yang terdapat pada manusia normal) menjadi PrPsc, yaitu molekul prion yang infektif, yang diperkirakan menjadi sebab timbulnya CJD secara sporadis.
Oleh karena itu, dapat disimpulkan bahwa penyakit asal prion pada manusia bersifat menular sekaligus juga diturunkan. Bukti mengenai interaksi antara sifat genetik dan iniektif tersebut dengan jelas ditunjukkan melalui hasil percobaan pada mencit yang gen PrPnya telah dibuang. Mencit itu ternyata manjadi resisten terhadap infeksi prion dan tidak mampu menghasilkan partikel-partikel prion yang infektif.
Masalahnya sekarang adalah: Bagaimana prion yang infektif (PrPsc) itu memperbanyak diri? Sejauh ini pencarian asam nukleat yang spesifik dibawa oleh prion tidak membuahkan hasil. Meskipun demikian, satu hal yang telah diketahui adalah bahwa replikasi prion yang infektif merupakan proses eksponensial yang melibatkan proses pasca translasi dari PrPc atau molekul prekursor lain menjadi PrPsc.
Berdasarkan pengetahuan yang ada, telah diusulkan berbagai model multiplikasi prion. Salah satu dari model itu melibatkan pembentukan kompleks antara PrPsc dengan protein ismorfnya (PrPc) yang terdapat pada sel manusia sehat membentuk kompleks PrPsc –PrPc.
Melalui kompleks molekul itu terjadi perubahan konformasi yang mengubah PrPc menjadi PrPsc, sehingga dari satu molekul PrPsc terbentuk dua molekul PrPsc. Kedua molekul prion infektif itu selanjutnya membentuk pasangan lagi dengan PrPc. Siklus pembentukan kompleks dan konversi molekuler itu berlangsung berkali-kali sehingga terjadi perbanyakan prion secara eksponensial, meskipun prion itu sendiri tidak mempunyai bahan genetik kenvensional.
Perubahan PrPc menjadi PrPsc nampaknya lebih disebabkan karena perubahan struktur proteinnya. Hasil analisis biofisika protein menunjukkan bahwa PrPsc mempunyai lebih banyak struktur betasheet daripada molekul PrPc. Oleh karena itu, teori yang ada pada umumnya sepakat bahwa pembentukan PrPsc dari PrPc karena konversi alpha-heliks menjadi beta-sheet.
Penyakit prion bersifat genetik karena setiap sel hewan atau manusia mempunyai gen yang menyandikan protein PrPc yang menjadi substrat PrPsc untuk multiplikasi. Selain itu, gen PrPc dapat mengalami mutasi sehingga PrPc berubah menjadi PrPsc.
Penyakit ini juga menular karena partikel PrPsc dapat dipindahkan dari satu individu ke individu lain seperti yang terjadi pada transmisi mikroorganisme, virus, dan viroid. Meskipun dalam hal transmisinya prion mirip dengan virus atau viroid tetapi prion hanya berupa protein.
Hal ini yang menyebabkan sulit diterimanya konsep prion pada masa awalnya, karena secara biokimia dan genetika proses reproduksi atau replikasi selalu melibatkan asam nukleat. Nyatanya partikel prion tersusun sebagian besar, jika tidak seluruhnya dari isomorf protein yang tidak normal yaitu PrPsc, entah karena mutasi PrPc atau karena konversi PrPc oleh prion infektif.
Boikot daging sapi Inggris
Multiplikasi prion yang tidak umum (karena melibatkan interaksi protein-protein) akan menjadi paradigma baru dalam kawasan riset dasar dan biomedis. Biologi prion pada mulanya berakar pada virologi dan neuropatologi, tetapi hubungannya dengan biologi molekuler dan kimia protein baru akhir-akhir ini disadari.
Oleh karena itu, studi mengenai multiplikasi prion dan penyakit yang ditimbulkannya akan sangat tergantung pada ilmu-ilmu itu, dan akan membuka cakrawala baru dalam biokimia dan genetika.
Partikel prion penyebab CJD atau panyakit asal prion lain pada manusia mungkin saja berbeda dengan penyebab BSE. Sejauh ini nampaknya juga belum ada bukti yang kuat bahwa infeksi prion penyebab BSE pada manusia menjadi satu-satunya pemicu timbulnya CJD.
Jika demikian, mengapa terjadi boikot besar-besaran terhadap daging sapi Inggris?
Sebagaimana telah dikemukakan, penyakit prion erat hubungannya dengan mutasi pada gen PrPc manusia yang masih belum banyak diketahui mekanismenya. Induksi gen yang semula dalam keadaan tidur sudah banyak dilaporkan, dan seringkali dapat bersifat fatal sebabagaimana yang terjadi pada ekspresi sejumlah gen-gen penyebab kanker.
Karena itu, tidak tertutup kemungkinan terbentuknya sejumlah prion baru yang mungkin akan lebih berbahaya dan lebih serasi dalam menginfeksi inang yang baru.
Selain itu, prion bersifat dapat menular. Usaha-usaha untuk menangkal penyebaran prion sebagaimana telah dilakukan oleh sejumlah negara merupakan langkah preventif yang dari segi ilmiah juga dapat dipertanggungjawabkan. Sudahkah kita siap untuk menyediakan payung sebelum hujan dalam kasus mad cow ini?
(Antonius Suwanto, dosen Jurusan Biologi, FMIPA IPB dan staf peneliti PAU Bioteknologi IPB)
Sumber: Kompas, Kamis, 11 April 1996